CaCO3 + CO2 + H2O → Ca(HCO3)2 là phản xạ hóa phù hợp. Bài viết lách này hỗ trợ không thiếu vấn đề về phương trình chất hóa học đang được thăng bằng, ĐK những hóa học nhập cuộc phản xạ, hiện tượng kỳ lạ (nếu có), ... Mời chúng ta đón xem:
Phản ứng CaCO3 + CO2 + H2O → Ca(HCO3)2
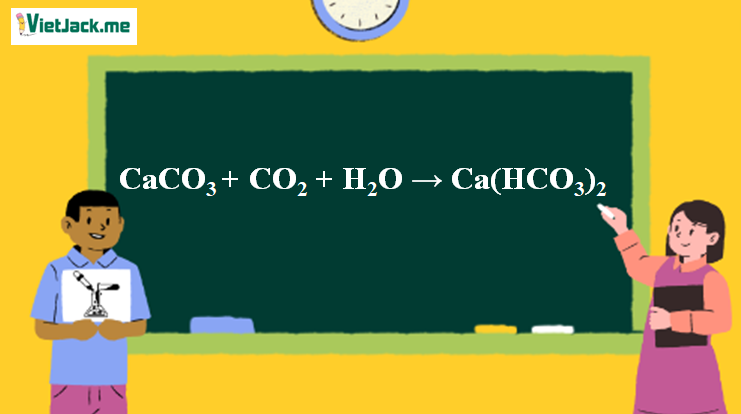
1. Phương trình phản xạ CaCO3 rời khỏi Ca(HCO3)2
CaCO3 + CO2 + H2O → Ca(HCO3)2
2. Điều khiếu nại phản xạ CaCO3 tính năng với CO2
Nhiệt phỏng thường
3. Bản hóa học của CaCO3 (Canxi cacbonat) vô phản ứng
CaCO3 là muối bột cacbonat phản ứng được với nước sở hữu hòa tan CO2 sẽ tạo trở thành Ca(HCO3)2 tan nội địa. (Chú ý: Đây là phản xạ thuận nghịch tặc tạo nên thạch nhũ vô hố động)
4. Mở rộng lớn kiến thức và kỹ năng về CaCO3
4.1. Tính hóa học vật lí và nhận biết
- Tính hóa học vật lí: Là hóa học rắn white color, ko tan nội địa.
- Nhận biết: dùng hỗn hợp axit HCl, thấy bay rời khỏi khí ko màu sắc, ko mùi:
CaCO3 + 2HCl → CaCl2 + H2O + CO2
4.2. Tính hóa học hóa học
- Mang không thiếu đặc thù chất hóa học của muối:
Tác dụng với axit mạnh:
CaCO3 + 2HCl → CaCl2 + H2O + CO2
Kém bền với nhiệt:
CaCO3 -to→ CaO + CO2
CaCO3 tan dần dần nội địa sở hữu hòa tan khí CO2.
CaCO3 + CO2 + H2O ⇆ Ca(HCO3)2
→ Khi đun nóng:
Ca(HCO3)2 -to→ CaCO3↓ + CO2 + H2O
4.3. Điều chế
Đa số cacbonat can xi được dùng vô công nghiệp là được khai quật kể từ đá mỏ hoặc đá núi. Cacbonat can xi tinh nghịch khiết (ví dụ loại dùng để dung dịch hoặc dược phẩm), được pha trộn kể từ mối cung cấp đá mỏ (thường là cẩm thạch) hoặc nó hoàn toàn có thể được dẫn đến bằng phương pháp mang lại khí cacbonic qua quýt hỗn hợp can xi hidroxit.
Ca(OH)2 + CO2 → CaCO3↓ + H2O
4.4. Ứng dụng
+ CaCO3 được coi như thể hóa học phụ gia mang lại ngành phát hành thành phầm thực phẩm chăn nuôi mang lại gia súc. Trong khi, Canxi cacbonat cũng chính là mối cung cấp đủ dinh dưỡng quan trọng mang lại quy trình tạo hình trứng và sự cải tiến và phát triển của xương so với những loại gia ráng.
+ CaCO3 được dùng như một loại phân bón chung cây cối cải tiến và phát triển, ổn định quyết định phỏng pH mang lại khu đất, hỗ trợ dưỡng chất mang lại cây.
+ Dường như, CaCO3 còn được dùng như hóa học phụ gia mang lại ngành phát hành dung dịch trừ thâm thúy vày loại khoáng này khá thân thiết thiện với môi trường xung quanh.
5. Tính hóa chất của CO2
CO2 là oxit axit
- CO2 tan nội địa tạo nên trở thành axit cacbonic (là một điaxit đặc biệt yếu)
CO2 + H2O ↔ H2CO3
- CO2 tính năng với oxit bazơ → muối bột.
CaO + CO2 → CaCO3 (t0)
- CO2 tính năng với hỗn hợp bazơ → muối bột + H2O
NaOH + CO2 → NaHCO3
2NaOH + CO2 → Na2CO3 + H2O
- CO2 bền, ở sức nóng phỏng cao thể hiện tại tính lão hóa Khi tính năng với những hóa học khử mạnh
CO2 + 2Mg → 2MgO + C
CO2 + C → 2CO
Lưu ý: Được dùng để làm lý giải CO2 ko dùng để làm dập tắt những vụ cháy nổ sắt kẽm kim loại.
6. Câu chất vấn áp dụng
Câu 1. Cho phương trình chất hóa học sau: CaCO3 + CO2+ H2O ⇌ Ca(HCO3)2
Phương trình chất hóa học bên trên là phản ứng
A. tạo nên thạch nhũ vô hố động
B. tạo nên macma
C. tạo nên muối bột CaCl2
D. tạo nên kết tủa xanh xao lam
Lời giải:
Đáp án: A
Câu 2. Quá trình tạo nên trở thành thạch nhũ trong những hố động đá vôi kéo dãn mặt hàng triệu năm. Quá trình này được lý giải vày phương trình chất hóa học này tại đây ?
A. Ca(HCO3)2 → CaCO3 + CO2 + H2O
B. Mg(HCO3)2 → MgCO3 + CO2 + H2O
C. CaCO3 + CO2 + H2O → Ca(HCO3)2
D. CaCO3 + 2H+ → Ca2+ + CO2 + H2O
Lời giải:
Đáp án: A
Giải thích:
Quá trình tạo nên thạch nhũ vô hố động là do: Ca(HCO3)2 → CaCO3 + CO2 + H2O.
phản ứng nghịch: CaCO3 + CO2 + H2O → Ca(HCO3)2 lý giải sự xâm thực của nước mưa
Câu 3. Phản ứng chất hóa học xẩy ra vô quy trình tạo nên thạch nhũ trong những hố động đá vôi là
A. CaCO3 + CO2 + H2O → Ca(HCO3)2
B. Ca(OH)2+ CO2 → CaCO3 + H2O
C. Ca(HCO3)2→ CaCO3+ CO2 + H2O
D. Ca(OH)2 + 2CO2 → Ca(HCO3)2
Lời giải:
Đáp án: C
Câu 4. Dẫn luồng khí CO qua quýt láo phù hợp bao gồm Fe2O3, CuO, MgO, Al2O3 (nung nóng). Sau Khi phản xạ xẩy ra trọn vẹn chiếm được hóa học rắn là
A. Al2O3, Cu, MgO, Fe.
B. Al, Fe, Cu, Mg.
C. Al2O3, Cu, Mg, Fe.
D. Al2O3, Fe2O3, Cu, MgO.
Lời giải:
Đáp án: A
Xem tăng những phương trình phản xạ chất hóa học khác:
CaOCl2 + HCl → CaCl2 + Cl2 + H2O
CaOCl2 → CaCl2 + O2
H2SO4 + KOH → K2SO4 + H2O
KOH + HCl → KCl + H2O
KOH + H3PO4 → K3PO4 + H2O
